
Schweres akutes respiratorisches Syndrom Coronavirus 2 (SARS-CoV-2) ist ein kürzlich identifizierter Coronavirus-Stamm, der für die Coronavirus-Krankheit 2019 (COVID-19) und die Pandemie verantwortlich ist. SARS-CoV-2 entstand im Dezember 2019 in China und wird hauptsächlich über Tröpfchen und Oberflächenkontaktwege übertragen. Symptome können Anzeichen und Symptome einer akuten Atemwegserkrankung wie Fieber, Husten, Kurzatmigkeit sein, aber die Infektion kann auch asymptomatisch sein. Das Virus infiziert menschliche Zellen durch Interaktion mit dem Angiotensin-Converting-Enzym 2 (ACE2) auf der Oberfläche von Atmungszellen und Spike(S)-Protein auf der äußeren Hülle des Virion-Partikels, insbesondere mit seiner Rezeptorbindungsdomäne (RBD). Das Spike (S)- und das Nukleokapsidprotein (NC) sind die Hauptimmunogene von SARS-CoV-2. Antikörper gegen die RBD des S-Proteins gelten als neutralisierend aktiv, da sie die Interaktion mit dem ACE2-Rezeptor blockieren und dadurch die zelluläre Infiltration blockieren können. Während sich die wissenschaftliche Gemeinschaft seit einiger Zeit auf diese neutralisierenden Antikörper konzentriert, werden das Auftreten von immun-evasiven Varianten und die ersten Studien, zur Entwicklung von Impfstoffen mit dem Nukleokapsid von SARS-CoV-2, die Notwendigkeit schaffen, beide Antikörperspezies zu bestimmen.
Deshalb haben wir uns entschieden, mit unserer FluoBolt™-Technologie den ersten Quantitativen Duplex-Antikörpertest (DAT) für Antikörper gegen SARS-CoV-2 zu entwickeln.
Der „Cov19 FluoBoltTM-DAT“ (Art. Nr. FIA-1707-FC5) ermöglicht die gleichzeitige und quantitative Bestimmung von Antikörpern gegen das S1RBD- UND Nukleokapsid-antigen von SARS-CoV-2 innerhalb einer einzigen Messung unter Verwendung von nur 10 μl Probe und liefert Ergebnisse innerhalb von 60 Minuten.
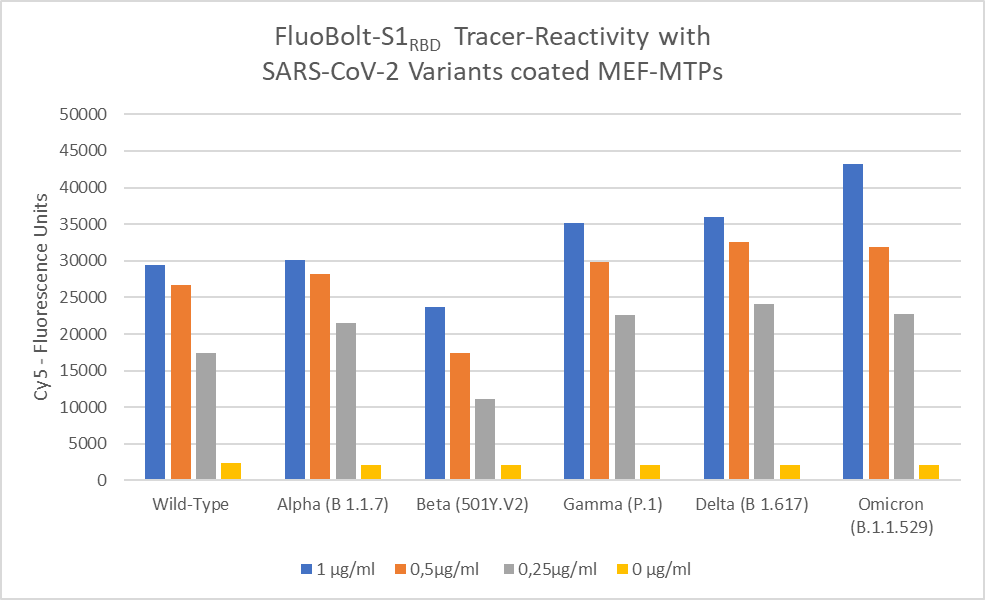
Im Gegensatz zu anderen Antikörper-Assays, die alle gegen das S1- oder NC-Protein erzeugte Antikörper nachweisen, ist der „Cov19 FluoBoltTM-DAT“ epitop-spezifisch und detektiert immundominante Antikörperspezies, d.h. die wichtigsten Antikörper, die entweder durch Impfung oder Infektion entstehen. Dies zeigt sich auch sehr gut darin, dass der Assay Anti-S1RBD Antikörper gegen alle bisher identifizierten dominanten Virusvarianten erkennt (siehe Grafik unten):
Daher kann der „Cov19 FluoBoltTM-DAT“ Assay ein wertvolles Werkzeug sein, um ein antikörperbasiertes „Schutzkorrelat“ zu etablieren, d.h. zu bestimmen welche Menge und Art des Antikörpers für einen bestimmten Zeitraum Schutz bietet.
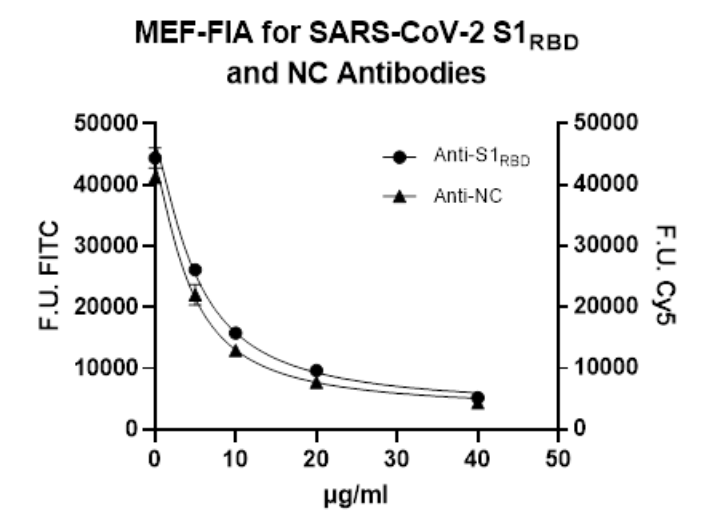
Anti-S1RBD- und Anti-NC-Antikörper, die in Serum- oder Plasmaproben von Patienten vorhanden sind, konkurrieren mit analogen fluoreszenzmarkierten Antikörpern (FITC und Cy5-markiert) um die Bindungsstellen des NC-Protein und der S1RBD-Domäne, die auf eine Metal Enhanced Fluorescence-Mikrotiterplatte (MEF-MTP) beschichtet sind. Es besteht ein direkter Zusammenhang zwischen der Menge an SARS-CoV-2-Antikörpern in der Probe und der Menge an Fluoreszenzeinheiten (FUs), die mit einem Fluoreszenz-Mikroplattenlesegerät gemessen werden. Kalibratoren mit bekannter Menge an Anti-S1RBD- und Anti-NC-Antikörpern werden verwendet, um Kalibrierkurven zu erstellen und so die Antikörperkonzentration einer unbekannten Probe zu quantifizieren.
Impact of SARS-CoV-2 variant-associated RBD mutations on the susceptibility to serum antibodies elicited by COVID-19 infection or vaccination. Chen LL et al., Clin Infect Dis. 2021 Jul 26: doi: 10.1093/cid/ciab656. Online ahead of print.
Neutralizing antibodies against SARS-CoV-2 variants induced by natural infection or vaccination: a systematic review and pooled meta-analysis. Chen X et al Clin Infect Dis. 2021 Jul 24:ciab646. doi: 10.1093/cid/ciab646. Online ahead of print.
Antibody response to SARS-CoV-2 infection in humans: A systematic review. Post N et al., PLoS One. 2020 Dec 31;15(12):e0244126.
The Nucleocapsid protein triggers the main humoral immune response in COVID-19 patients. Smits VAJ et al., Biochem Biophys Res Commun. 2021 Mar 5;543:45-49
Anti-spike, Anti-nucleocapsid and Neutralizing Antibodies in SARS-CoV-2 Inpatients and Asymptomatic Individuals.
Brochot E. et al., Front Microbiol. 2020 Oct 19;11:584251
The SARS-CoV-2 spike protein: balancing stability and infectivity. Berger I, Schaffitzel C. Cell Res. 2020 Dec;30(12):1059-1060. doi: 10.1038/s41422-020-00430-4. PMID: 33139926; PMCID: PMC7604330
Ju B, Zhang Q, Ge J, et al. Human neutralizing antibodies elicited by SARS-CoV-2 infection. Nature. 2020 Aug;584(7819):115-119. doi: 10.1038/s41586-020-2380-z. Epub 2020 May 26. PMID: 32454513.
© 2025 All Rights Reserved.